恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化疗效的Meta分析

王佳坤
 , 檀岭改, 陈德志, 林冠, 杨昌云, 甘惠贞
, 檀岭改, 陈德志, 林冠, 杨昌云, 甘惠贞
解放军第180医院药学科,泉州 362000
作者简介 王佳坤(1985-),男,福建惠安人,主管药师,学士,研究方向:临床药学。电话:0595-28919452,E-mail:wangjiakun0407@126.com。
通信作者 甘惠贞(1973-),女,福建龙海人,主管药师,学士,研究方向:药事管理。电话:0595-28919451,E-mail:13599220436@139.com。
中图分类号: R978.7 文献标识码: B 文章编号: 1004-0781(2016)04-0418-07
摘要:
目的 评价恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化的疗效。方法 计算机检索PubMed、Embase、The Cochrane Library和中国知网、维普数据库、万方数据库等文献数据库,查找恩替卡韦联合安络化纤丸治疗乙型肝炎纤维化的随机对照试验,检索时间从建库至2014年11月。由2位研究者按纳入和排除标准独立进行文献筛选,资料提取,并对其进行质量评价,采用RevMan5.2版软件进行Meta分析。结果 符合纳入标准的文献共有10篇,包括653例患者。Meta分析结果,恩替卡韦联合安络化纤丸可明显降低患者的血清透明质酸[MD=-96.46,95%CI(-127.89,-65.03)]、血清层粘连蛋白[MD=-50.72,95%CI(-65.54,-35.89)]、Ⅲ型前胶原[MD=-74.46,95%CI(-96.74,-52.18)]、Ⅳ型胶原[MD=-57.03,95%CI(-78.74,-35.32)]和丙氨酸氨基转移酶[MD=-8.14,95%CI(-10.62,-5.65)]。结论 恩替卡韦联合安络化纤丸可以明显改善肝纤维化4项指标和丙氨酸氨基转移酶。
关键词: 恩替卡韦 ; 安络化纤丸 ; 肝纤维化 ; 对照试验 ; 随机 ; Meta分析
世界范围内超过35亿人为慢性乙型肝炎病毒(hepatitis B virus,HBV)携带者,其中约25%最终发生肝硬化。据统计,每年死于慢性乙型肝炎(chronic hepatitis B,CHB)及其并发病者约100万例,代偿性肝硬化5年死亡率16%,失代偿性肝硬化5年死亡率86%。肝硬化是肝脏弥漫性病变损伤的终末期常见表现,是严重危害人类健康的常见病之一,而肝纤维化贯穿于慢性乙肝的基本临床过程[1]。早期干预、阻止肝纤维化的进展是预防肝病发展为肝硬化的关键[2]。目前认为,对CHB患者给予抗病毒治疗是延续和阻止肝纤维化的关键措施。恩替卡韦(entecavir,ETV)临床应用起效快、耐药突变率低,目前已被临床广泛应用,并被证实可有效缓解肝纤维化及早期肝硬化的进展[3]。安络化纤丸作为国家食品药品监督管理总局批准用于治疗肝硬化的中成药,具有疏通肝血流、清除肝内淤积、促使肝纤维降解和吸收的作用[4]。近年来,临床上采用恩替卡韦联合安络化纤丸治疗CHB肝纤维化报道日益增多,并有不少文献报道其对乙型肝炎肝纤维化有较好的疗效,但是对其确切疗效及是否能减缓CHB患者肝硬化过程尚未得到系统评价。笔者在本研究中按照Cochrane系统评价方法,对恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化疗效进行Meta分析,以期为临床应用和进一步研究提供最佳证据。
1 资料与方法
1.1 纳入和排除标准
1.1.1 研究类型 国内外关于恩替卡韦联合安络化纤丸治疗CHB的随机对照试验(randomized controlled trial,RCT),无论是否采用盲法或分配隐藏。
1.1.2 研究对象 临床诊断为CHB患者,诊断符合2000年9月 《病毒性肝炎防治方案》中的诊断标准[5]。
1.1.3 干预措施 试验组采用恩替卡韦联合安络化纤丸,对照组采用恩替卡韦。
1.1.4 排除标准 ①动物实验及非原始文献;②排除合并其他感染、有严重心脑血管疾病、严重呼吸系统疾病、肝肾器官功能障碍和糖尿病;③文献试验组干预措施除恩替卡韦和安络化纤丸外,还给予对照组未使用的其他治疗方法;④未设计对照或以自身对照;⑤重复发表的文献或数据不完整而无法提取的文献。
1.2 结局指标
1.2.1 主要指标 血清肝纤维化指标血清玻璃酸(hyaluronic acid,HA)、血清层粘连蛋白(laminin,LN)、Ⅲ型前胶原(procollagen type Ⅲ,PCⅢ)、Ⅳ型胶原(collagenase type Ⅳ,Ⅳ-C)。
1.2.2 次要结局指标 丙氨酸氨基转移酶(alanine transaminase,ALT)、HBV-DNA转阴率。
1.3 资料检索
采用计算机检索,检索资料库包括:PubMed、Embase、The Cochrane Library和中国知网(CNKI)、维普数据库(VIP)、万方数据库(WanFang Data)。文献检索无语言限制,检索日期截止2014年11月。中文检索词包括:“恩替卡韦”“安络化纤丸”“乙型肝炎”“肝硬化”“肝纤维化”“随机”;英文检索词:“entecavir”“anluohuaxian”“hepatitis B”,根据不同资料库的特征分别进行主题词联合自由词、关键词,篇名联合全文进行综合检索。
1.4 文献筛选与资料提取
由2位研究者按照纳入和排除标准独立筛选文献,用事先设计的资料提取表格提取信息,内容包括:①纳入研究的一般特征及基本情况;②反应研究质量的指标;③干预措施具体的使用方法;④临床结局指标。如遇分歧,讨论解决。如研究报告的资料不全,则进一步与作者联系获取。
1.5 文献质量评价
对纳入本研究的RCT质量采用Cochrane RevMan’s Handbook 5.1.0随机对照试验的偏倚风险评估工具进行评价:①随机分配方法;②分配方案隐藏;③对研究的参与者和相关人员使用盲法;④研究结果测量采用盲法;⑤结果数据的完整性;⑥选择性报告研究结果;⑦其他偏倚来源;针对每一项研究结果,对上述7条作出“是”(低度偏倚)、“否”(高度偏倚)和“不清楚”(缺乏相关信息或偏倚情况不确定)的判断[6]。
1.6 统计学方法
采用Cochrane协作网提供的RevMan 5.2版软件进行资料的统计分析。各临床试验的异质性检验采用χ2检验;若无统计学异质性(P>0.1,I2>50%),选择固定效应模型进行Meta分析,否则选择随机效应模型或进行定性的系统评价。Meta分析结果讨论的依据为RevMan软件的森林图,计量资料采用均数差(mean difference,MD)或标准化均数差(standardized mean difference,SMD)及其95%可信区间((confidence interval,CI),计数资料采用相对危险度(relative risk,RR)或比值比(odds ratio,OR)及其95%CI,检验水准为α=0.05。
2 结果
2.1 文献检索结果
根据制定的检索词检索出相关文献159篇,其中中国知网 118篇、重庆维普数据库 20篇、万方数据库21篇;剔除重复文献后,获得文献118篇,根据题录和摘要,初步纳入相关文献20篇;进一步阅读全文,最终根据文献纳入、排除标准确定纳入RCT 10篇,全部为中文文献,发生地在中国,共纳入CHB患者653例,其中治疗组337例,对照组316例。纳入文献的基本特征见表1。
表1 纳入文献的基本特征
2.2 纳入研究的质量评价
见表2。
表2 纳入研究的方法学质量评价
2.3 Meta分析结果
2.3.1 HA 10个研究均报道了HA,根据疗程不同分为疗程6个月、48周、12个月3个亚组进行Meta分析[6]。结果显示,疗程48周研究结果间有统计学异质性(P=0.006,I2=81%),疗程12个月结果间有统计学异质性(P<0.000 01,I2=91%),均对其异质性进行分析后发现,其异质性可能与各试验中患者肝硬化程度构成比不一致有关;故采用随机效应模型进行Meta分析,疗程6个月MD=-45.92,95%CI(-63.06,-28.78),疗程48周MD=-88.39,95%CI(-141.22,-35.55),疗程12个月MD=-109.36,95%CI(-141.63,-77.09);3组合并后MD=-96.46,95%CI(-127.89,-65.03),两组降低HA的差异有统计学意义,表明治疗组降低HA的疗效优于对照组。见图1。

图1 两组HA治疗前后差值比较的Meta分析结果
2.3.2 LN 10个研究均报道了LN,根据疗程不同分为疗程6个月、48周、12个月3个亚组进行Meta分析[4,8-16]。结果显示,疗程48周研究结果间有统计学异质性(P=0.02,I2=76%),疗程12个月结果间有统计学异质性(P=0.001,I2=75%),均对其异质性进行分析后发现,其异质性可能与各试验中患者肝硬化程度构成比不一致有关;故采用随机效应模型进行Meta分析,疗程6个月MD=-45.40,95%CI(-66.03,-24.77),疗程48周MD=-81.06,95%CI(-115.61,-46.51),疗程12个月MD=-39.50,95%CI(-53.25,-25.76);3组合并后MD=-50.72,95%CI(-65.54,-35.89),两组降低LN的差异有统计学意义,表明治疗组降低LN的疗效优于对照组。见图2。
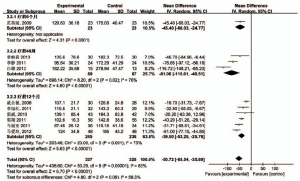
图2 两组LN治疗前后差值比较的Meta分析结果
2.3.3 PCⅢ 10个研究均报道了PCⅢ,根据疗程不同分为疗程6个月、48周、12个月3个亚组进行Meta分析[4,8-16]。结果显示,疗程48周研究结果间有统计学异质性(P=0.000 5,I2=87%),疗程12个月结果间有统计学异质性(P<0.000 01,I2=90%),均对其异质性进行分析后发现,其异质性可能与各试验中患者肝硬化程度构成比不一致有关;故采用随机效应模型进行Meta分析,疗程6个月MD=-34.89,95%CI(-52.05,-17.73),疗程48周MD=-105.34,95%CI(-147.30,-63.38),疗程12个月MD=-66.39,95%CI(-91.76,-41.03);3组合并后MD=-74.46,95%CI(-96.74,-52.18),两组降低PCⅢ的差异有统计学意义,表明治疗组降低PCⅢ的疗效优于对照组。见图3。
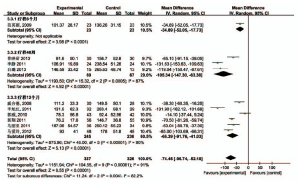
图3 两组PCⅢ治疗前后差值比较的Meta分析结果
2.3.4 Ⅳ-C 10个研究均报道了Ⅳ-C,根据疗程不同分为疗程6个月、48周、12个月3个亚组进行Meta分析[4,8-16]。结果显示,疗程48周研究结果间有统计学异质性(P<0.000 01,I2=91%),疗程12个月结果间有统计学异质性(P<0.000 01,I2=95%),均对其异质性进行分析后发现,其异质性可能与各试验中患者肝硬化程度构成比不一致有关;故采用随机效应模型进行Meta分析,疗程6个月MD=-34.89,95%CI(-52.05,-17.73),疗程48周MD=-105.34,95%CI(-147.30,-63.38),疗程12个月MD=-46..26,95%CI(-69.04,-23.47);3组合并后MD=-57.03,95%CI(-78.74,-35.32),两组降低PCⅢ的差异有统计学意义,表明治疗组降低PCⅢ的疗效优于对照组。见图4。
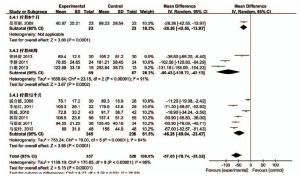
图4 两组Ⅳ-C治疗前后差值比较的Meta分析结果
2.3.5 ALT 8个研究报道了ALT,疗程为48周或12个月,各研究结果间无统计学异质性(P=0.14,I2=36%),采用固定效应模型进行Meta分析[3,8-13]。MD=-8.14,95%CI(-10.62,-5.65),两组差异有统计学意义,表明治疗组降低ALT的疗效优于对照组。见图5。
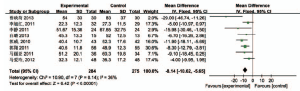
图5 两组ALT治疗前后差值比较的Meta分析结果
2.3.6 HBV-DNA转阴率 7个研究报道了HBV-DNA转阴率,根据疗程不同分为疗程6个月、48周、12个月3个亚组进行Meta分析[7-8,10,12-15]。结果显示,疗程48周研究结果间无统计学异质性(P=0.81>0.05),疗程12个月结果间无统计学异质性(P=0.90,I2=0%),采用固定效应模型进行Meta分析,疗程6个月OR=2.21,95%CI(0.36,13.47),疗程48周OR=1.30,95%CI(0.16,10.90),疗程12个月OR=1.16,95%CI(0.58,2.32),3组合并后OR=1.27,95%CI(0.69,2.35);两组差异无统计学意义,表明治疗组与对照组HBV-DNA转阴率相当。见图6。
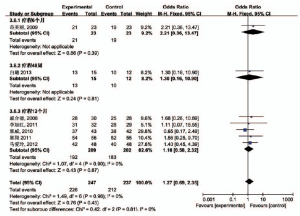
图6 HBV-DNA转阴率疗效比较
2.3.7 倒漏斗图分析 以2组HA治疗前后差值比较作倒漏斗图,结果见图7;倒漏斗图显示分布不完全对称,考虑可能主要与各实验的样本量较小有关,同时与存在发表偏倚(阴性结果的实验可能未发表)及方法学质量低下有关。
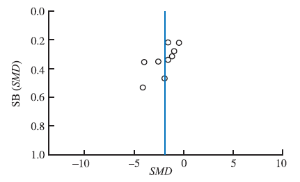
图7 两组HA治疗前后差值比较Meta分析倒漏斗图
3 讨论
肝纤维化是临床上较常见的慢性肝炎病理改变,HBV活动性复制,引起肝内慢性活动性炎症反应,是导致肝组织持续受损、逐步进展为肝硬化的根本原因,所以抗病毒治疗是阻止肝纤维化发生、发展的根本[15]。恩替卡韦是一种脱氧鸟嘌呤核苷类似物,能够强效选择性地抑制HBV的反转录酶,长期使用具有耐药率低、耐受性好等优点,是现有抗HBV作用最强的药物之一,对抗肝纤维化十分重要[16]。但抗肝纤维化治疗不仅仅是进行病因治疗,因为肝星状细胞(hepatic stellate cell,HSC)对肝纤维化的发展起重要作用,当肝发生炎症时,HSC活性增强,可使Ⅰ、Ⅲ型胶原的合成增加;抗病毒治疗不能完全代替抗肝纤维化治疗。安络化纤丸由地黄、三七、水蛭、地龙、牛黄、僵蚕等组成,主要功效为健脾养肝、凉血活血、软坚散结;具有疏通肝脏血流、消除肝脏炎症、促使肝纤维降解和吸收的作用,故可用于治疗慢性肝炎、早中期肝硬化[17]。安络化纤丸是通过抑制和溶解胶质纤维产生,阻断胶质纤维形成,阻止纤维化发展,激活胶质酶活性,加强分解纤维化能力,使已形成的纤维化加速降解吸收,并使部分硬化分解排泄,实现逆转纤维化[3]。
本研究遵循循证医学相关研究原则,对恩替卡韦联合安络化纤丸治疗乙肝肝纤维化的疗效进行Meta分析;本次系统评价纳入的10个RCT中有5个具有中度偏倚风险[7,11,13-15],纳入研究的方法学问题在于5个RCT的随机分配方法不明确[7,11,13-15],可能导致选择性偏倚的发生;10个RCT均提及分配隐藏方法,可能导致无法使患者治疗达到预期效果;5个RCT未提及盲法,可能在设计、资料收集或分析阶段出现信息偏畸[7,11,13-15]。
本系统评价结果显示,恩替卡韦联合安络化纤丸治疗乙肝肝纤维化,治疗组的HA、LN、PCⅢ和Ⅳ-C 4项指标与对照组相比均有明显降低,差异有统计学意义;在降低ALT方面,差异有统计学意义,治疗组的疗效优于对照组;在乙肝患者HBV-DNA转阴方面,差异无统计学意义。但由于以下几方面原因,解释这些结果需要慎重:①本研究中治疗组与对照组肝纤维化4项指标均存在异质性,可能与纳入研究的文献数量、RCT的样本量较少,使结果的偶然性增大有关;也可能与各试验中患者肝硬化程度构成比不一致有关;另外,纳入研究的方法学质量不高也是产生异质性的可能原因。②本次Meta分析只检索到中文文献,未检索到到外文文献,可能影响资料的全面性。③肝纤维化4项指标的临床意义有限。
综上所述,虽然目前已有的研究初步显示,恩替卡韦联合安络化纤丸可明显降低肝纤维化的4项指标和ALT,但由于本系统评价纳入的RCT较少、样本量较小,使结论的论证强度受到一定程度的限制。因此,进一步的研究有待于更加严谨设计的大样本、多中心、随机、对照试验,来进一步证实恩替卡韦联合安络化纤丸抗肝纤维化的疗效与安全性,以获取最佳证据。
The authors have declared that no competing interests exist.
参考文献
View Option
| [1] | 池肇春. 慢性乙型肝炎伴肝硬化抗病毒治疗[J]. | 中西医结合肝病杂志,2006,16(3):129-132.[本文引用:1] |
| [2] | 骆抗先. | 乙型肝炎基础和临床[M].3版.北京:人民卫生出版社,2006:227-231.[本文引用:1] |
| [3] | 曾映荷. 恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化的临床研究[J]. | 湖北中医杂志. 2013,35(6):11-12.[本文引用:5] |
| [4] | 侯金林.恩替卡韦:慢性乙型肝炎治疗的新选择[J]. | 肝脏,2005,10(2):164-166.[本文引用:4] |
| [5] | 中华医学会.病毒性肝炎防治方案[J]. | 中华传染病杂志,2001,19(1):56-62.[本文引用:1] |
| [6] | JULIAN P T, HIGGIN S, SALLY G. Cochrane Handbook for Systematic Reviews of Interventions[EB/OL]. | The Cochrane Collaboration,2013.. URL [本文引用:2] |
| [7] | 白璐. 恩替卡韦联合安络化纤丸治疗乙型肝炎肝硬化的临床观察[J]. | 中外健康文摘,2013,10(11):133.[本文引用:6] |
| [8] | 马爱玲,巩建华.恩替卡韦联合安络化纤丸治疗活动性乙型肝炎肝硬化疗效观察[J]. | 实用肝脏病杂志,2012,15(1):61-63.[本文引用:7] |
| [9] | 马丽亚. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝硬化的疗效观察[J]. | 临床医药实践,2011,20(5):348-349.[本文引用:2] |
| [10] | 李旭红,赖江琼,李奕鑫,等.恩替卡韦联合安络化纤丸治疗乙型肝炎肝硬化32例疗效分析[J]. | 传染病信息,2011,24(1):51-54.[本文引用:3] |
| [11] | 李静. 恩替卡韦联合安络化纤丸治疗乙肝后肝硬化失代偿期48例近期疗效观察[J]. | 医药论坛杂志,2011,32(16):154-156.[本文引用:5] |
| [12] | 郭翔. 恩替卡韦联合安络化纤丸治疗慢性乙型肝炎56例[J]. | 实用肝脏病杂志,2011,14(6):444-445.[本文引用:3] |
| [13] | 郭威,周莹,鲁有水,等.恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化43例[J]. | 医药导报,2010,29(9):1157-1159.[本文引用:6] |
| [14] | 范英丽,冯志成,袁勇.恩替卡韦联合安络化纤丸治疗乙肝肝纤维化23例临床研究[J]. | 云南中医中药杂志,2009,30(7):9-10.[本文引用:2] |
| [15] | 戚合德,杨阳,龚守军.安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化疗效观察[J]. | 中国现代医生,2008,46(11):88-89.[本文引用:7] |
| [16] | 慢性乙型肝炎抗病毒治疗专家委员会.慢性乙型肝炎抗病毒治疗专家共识[J]. | 中华实验和临床感染病杂志:电子版,2010,14(1):82-90.[本文引用:4] |
| [17] | 顾竹影,翁红雷,蔡卫民,等.探讨慢性肝炎患者血清肝纤维化指标的临床价值[J]. | 临床肝胆病杂志,2000,16(3):171-173.[本文引用:1] |

